前言
GPR61 是主要表达于垂体和大脑食欲调节中枢的A类孤儿G蛋白偶联受体,其与食欲和体重调节、儿童肥胖及2型糖尿病密切相关,是恶病质、肌少症等食欲缺乏相关疾病的潜在治疗靶点。但该受体存在内源性配体不明、作用机制未阐明的关键问题,且现有唯一反向激动剂存在活性低、选择性差等缺陷,同时缺乏可穿透血脑屏障的工具药验证其中枢调控作用,严重制约了该靶点的后续研究与药物开发。
同时,GPR61 尚无配体结合的结构解析,受体调控的分子基础缺失,无法为靶向药物设计提供理性依据。因此,开发强效、高选择性且可穿透血脑屏障的 GPR61 反向激动剂,并解析其与受体的复合物结构,成为探究该受体功能、验证其靶点价值的关键。
GPR61 是表达于垂体和大脑食欲调节中枢的 A 类孤儿 GPCR,与食欲体重调节、儿童肥胖及 2 型糖尿病相关,是恶病质等食欲缺乏疾病的潜在靶点。但该受体内源性配体不明、作用机制未阐明,现有反向激动剂存在活性低、选择性差等缺陷,也无穿透血脑屏障的工具药,制约了该靶点的后续研究与药物开发。
针对GPR61靶点,辉瑞开展了专项研究,旨在开发强效、高选择性且可穿透血脑屏障的反向激动剂,以治疗恶病质,目前项目处在临床前和早期药物发现阶段。
辉瑞研究团队Ethan L. Fisher 与 Yuan Zhang等人报道了一系列强效、高选择性GPR61 反向激动剂的发现与优化过程,核心成果包括:
新工具分子:通过筛选与优化获得化合物15、23等高活性、高选择性GPR61反向激动剂,为 GPR61 的药理学研究提供了核心工具。
新作用机制:首次解析了 GPR61 与反向激动剂结合的冷冻电镜结构,发现该类分子结合于细胞内别构口袋、阻断 Gαs 结合的全新 GPCR 反向激动模式。
新优化策略:明确 GPR61 调节剂的构效关系,发现仲磺酰胺叔胺化可显著提升脑穿透性,为GPR61调节剂的成药性改进指明方向。
相关研究以“Discovery of Potent and Brain-Penetrant Inverse Agonists for GPR61, an Orphan G Protein-Coupled Receptor”为题,于3月15日在线发表于《Journal of Medicinal Chemistry》。

研究内容
高通量筛选与构效优化
通过高通量筛选发现苗头化合物1,随后按 B 环→A 环→C 环的模块化思路进行构效关系研究,利用吡啶环与邻位甲基取代的协同效应逐步提升受体结合活性,最终得到理化性质平衡、纳摩尔级强效的 GPR61 反向激动剂化合物 15,并经靶点结合实验确认其与GPR61的特异性相互作用。
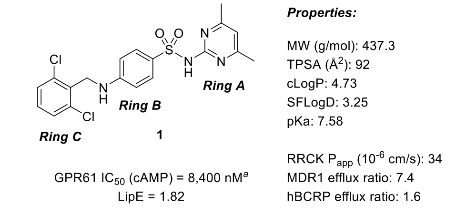
图1. 高通量筛选命中物(化合物 1)的结构及核心理化性质
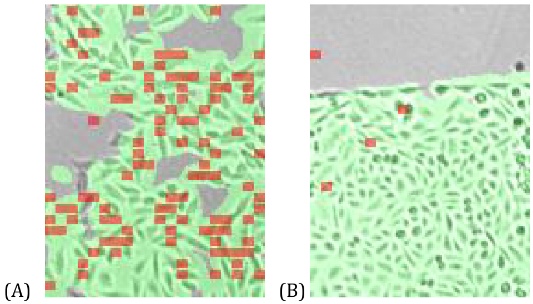
图2. SPRm验证化合物15与GPR61结合
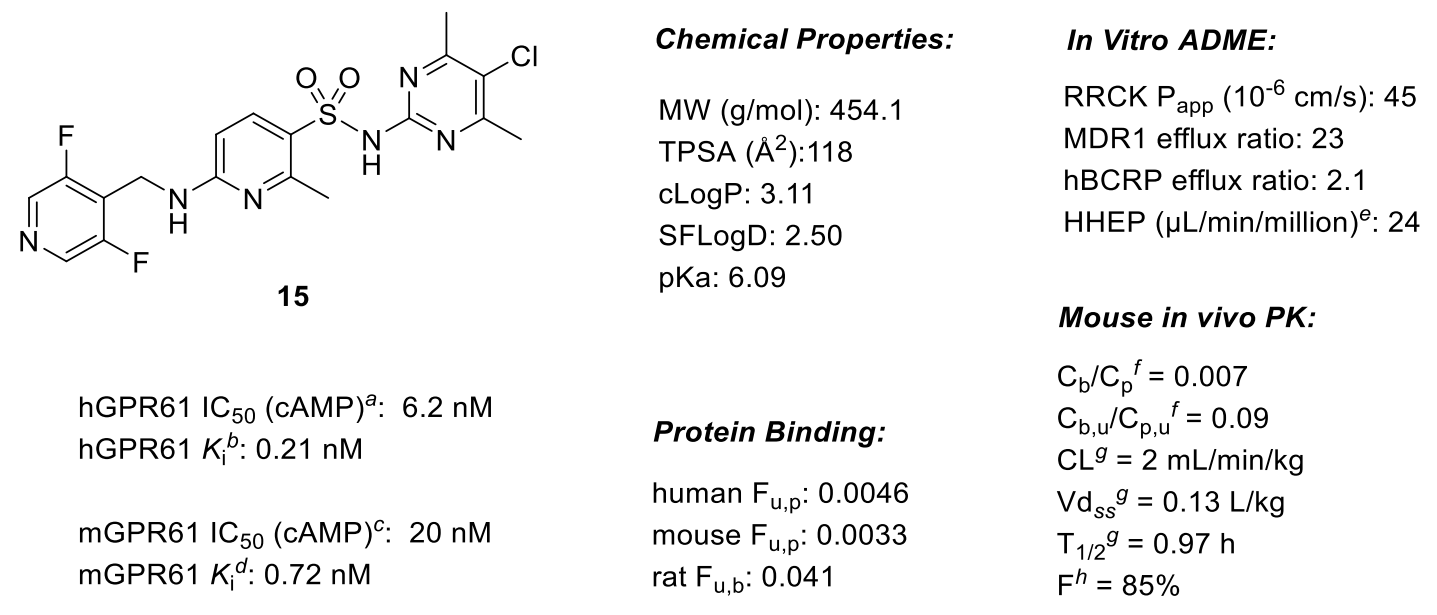
图3. 化合物15的性质与PK参数汇总
冷冻电镜结构揭示别构新机制
研究团队首次解析出 3.1 Å 分辨率的 GPR61与化合物15的冷冻电镜复合物结构,明确该类反向激动剂结合于受体诱导形成的细胞内别构口袋,通过物理阻断Gαs蛋白结合而抑制组成型活性,揭示了一种全新的 GPCR 反向激动作用模式,同时发现溶剂暴露的可修饰位点,为后续结构改造提供理性依据。
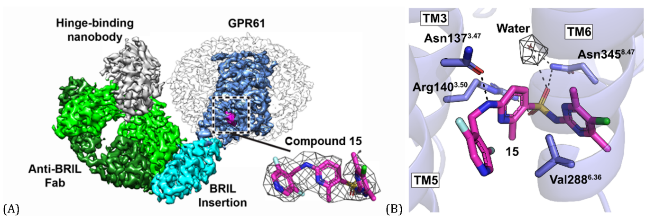
图4. GPR61 与化合物15结合的冷冻电镜结构
结构指导改善脑渗透性
基于结构解析发现的修饰位点,针对化合物15血脑屏障穿透性差的短板,将仲磺酰胺转化为叔磺酰胺进行结构改造;经侧链优化得到化合物23,其保持强效的GPR61 抑制活性,且MDR1 外排率显著降低,小鼠体内血脑屏障穿透性大幅提升,成为可穿透血脑屏障的工具分子,同时发现该化合物存在代谢清除率高、口服生物利用度低的成药性问题。
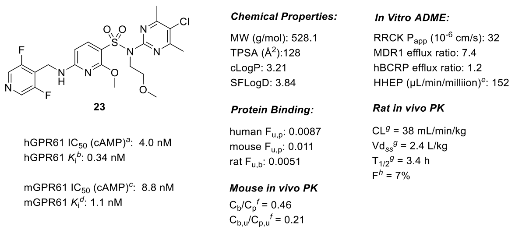
图5. 化合物23的性质与PK参数汇总
体内药代与药效验证
尽管化合物23在联合CYP抑制剂后实现高脑暴露和受体占据,但急性摄食实验未观察到促食欲效果,阳性对照药则表现出显著活性,提示 GPR61 的食欲调节机制仍需进一步阐明。
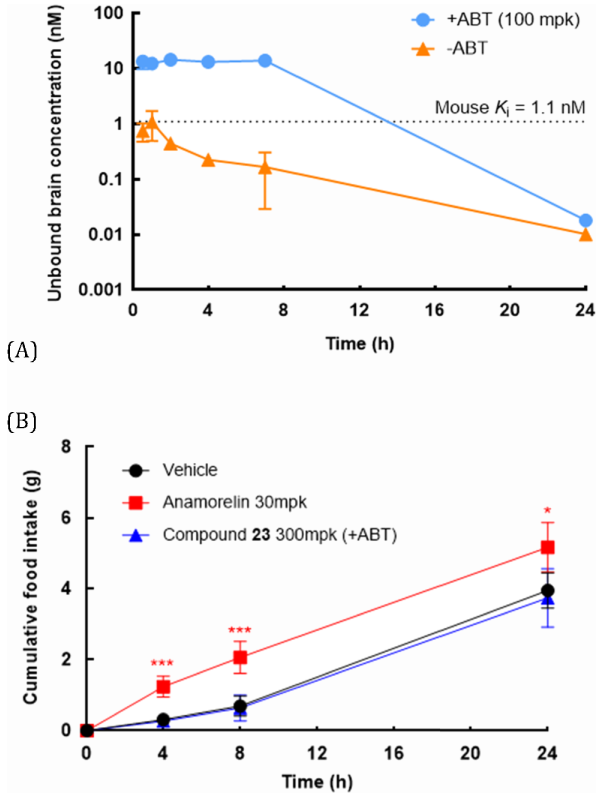
图6. 化合物23的急性摄食实验结果
总结
本研究通过系统的药物化学优化,成功发现了一类结构新颖的磺酰胺类 GPR61 反向激动剂,其中化合物15具有高活性、高选择性的特征,更重要的是,研究借助冷冻电镜技术首次解析了其与GPR61 的复合物结构,揭示了结合于受体细胞内诱导别构口袋、物理阻断G蛋白偶联的全新反向激动模式,丰富了GPCR 别构调节的理论体系。
基于结构指导的理性设计,研究团队通过仲磺酰胺向叔磺酰胺的改造得到化合物 23,实现了脑穿透性的突破性提升,成为首个可用于中枢研究的GPR61 工具分子。尽管受试化合物未在成年小鼠中观察到食欲调节效应,但其为后续GPR61 调节剂的研发提供了重要的工具化合物与优化思路。