对于药物研发而言,单晶X射线衍射是确证分子结构、绝对构型的“金标准”。
然而,药物合成过程往往存在诸多不可控因素,有时我们会得到粘稠、呈液态的油状分子。这类分子很难进行单晶培养,常常导致分子结构无法确证,致使接下来的研发工作陷入僵局。
#1哪些分子容易形成油状物?

在药物小分子合成与结构优化过程中,许多化合物都容易以油状形式存在,这一现象在小分子药物中间体、结构复杂的天然产物以及脂质类化合物中尤为普遍。从结构上看,这类分子往往具有低分子量、高柔性、弱极性及对称性差的特点。微弱的分子间作用力和极低的熔点,导致油状分子很难自发克服热运动进行有序排列。再加上它们极易包裹溶剂、阻碍分子进行紧密堆叠,因此,无论我们如何穷尽传统的单晶培养手段——不断调整溶剂配比、温度梯度或挥发速率——也往往难以成功诱导其形成规则晶格。
#2 两大核心技术,攻克油状分子难结晶难题
针对油状化合物这类传统方法难以结晶的情况,下面我们将介绍2种非常规的,但能有效解决难结晶问题的单晶培养手段,可以有针对性地解决油状分子无法培养单晶的技术难题。
1. 晶体海绵法:无需长单晶,直接锁定分子结构
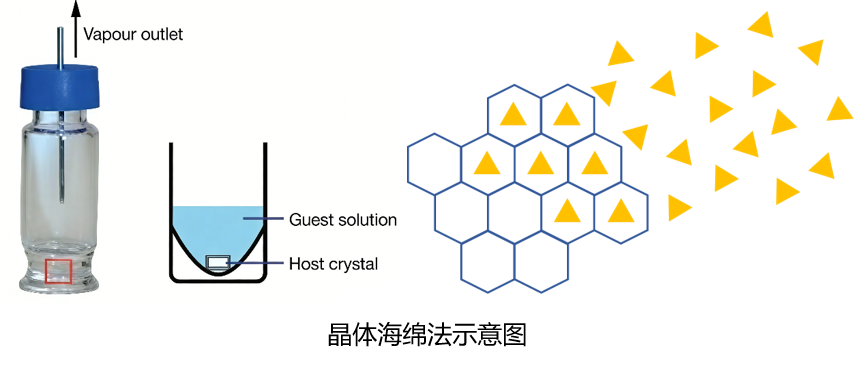
晶体海绵法是将提前结晶好的、具有均匀纳米孔道的多孔材料(晶体海绵)放入目标小分子溶液中,待油状目标小分子扩散、有序 “入住” 到海绵的孔道里,在孔道的限域作用下完成规则排列,就可以将载有样品的晶体直接进行X射线衍射分析,再扣除掉已知的海绵骨架结构,就能精准还原出目标分子的三维结构信息。[1]
哪些材料可以用作晶体海绵辅助结晶?
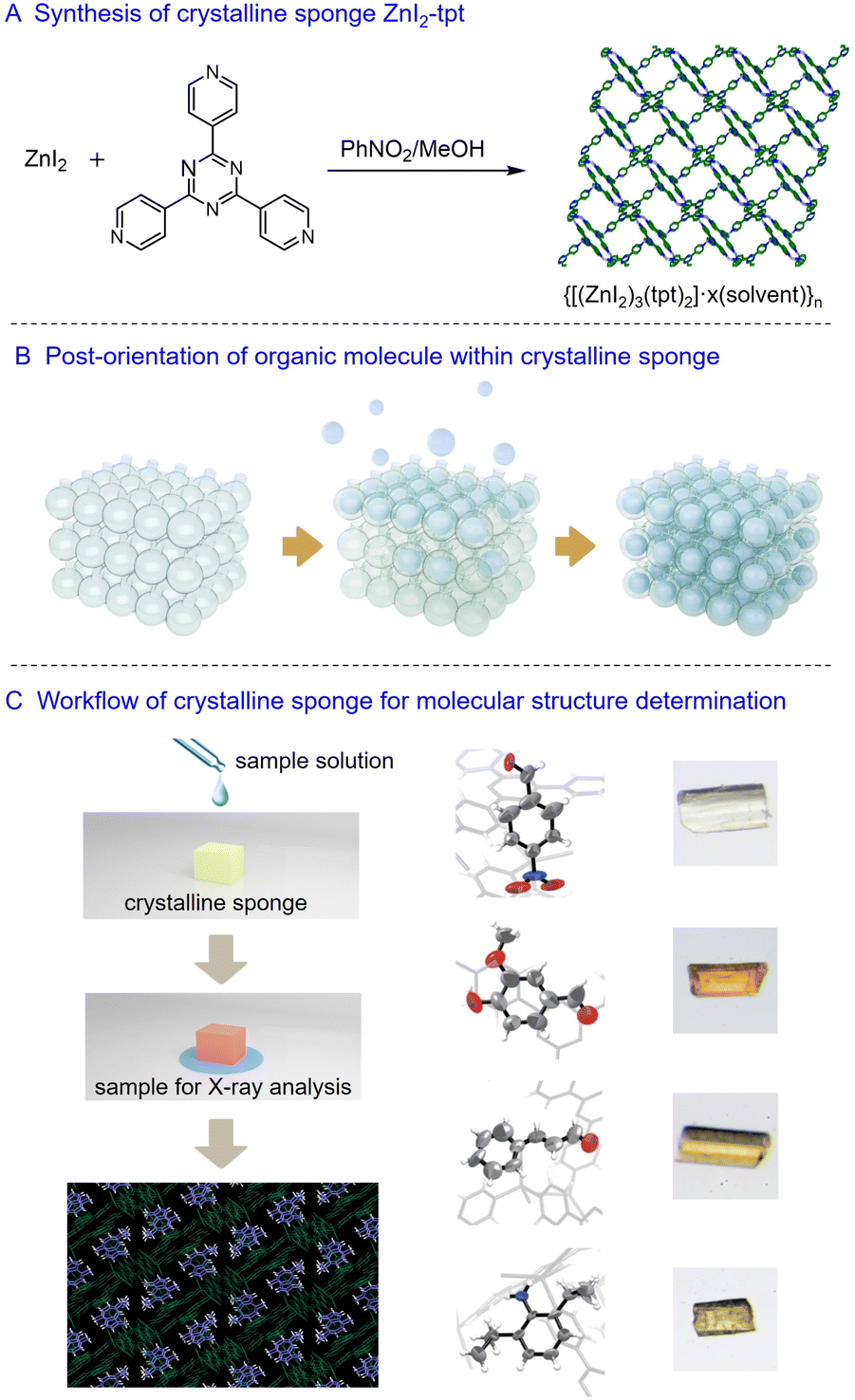
结晶海绵Znl2-tpt的合成 [5]
晶体海绵本质是具有均匀纳米孔道的多孔结晶材料,比较常见的是金属有机框架(MOF)材料,由金属离子与有机配体配位组装而成,具备孔径均一、结构稳定、比表面积大的特点。TPT-ZnI2、ZIF系列等均可作为晶体海绵用于油状分子的结构确证。此外,部分金属有机笼或超分子组装体在具备规整孔道、结构稳定且能实现单晶到单晶转换时,也可作为晶体海绵使用。[2]
晶体海绵法技术优势:
l 无需对目标分子进行单晶培养
l 样品消耗量低,降低研发成本
l 适用于油状分子、微量药物分子、难结晶固体粉末
青云瑞晶案例分享:
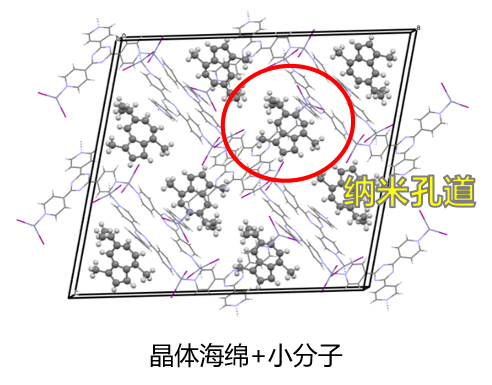

在晶体海绵法的案例中,针对某分子量仅200的油状药物分子,我们使用金属有机框架 TPT-ZnI₂作为“分子旅馆”,让油状分子有序 “入住” 其纳米孔道,全程无需单晶培养就成功确证了该药物分子的结构
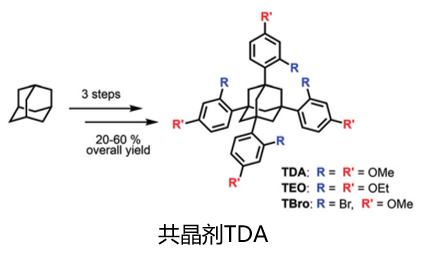
2. 共晶剂添加法:找对 “结晶伴侣”,轻松长出高质量单晶
如果说晶体海绵法是给分子准备现成的房子,共晶剂添加法就是给油状分子找一个会“排队”的好朋友,带着它一起形成规则的晶体。
 共晶剂添加法是引入一种结构已知、易于结晶的“伴侣分子”作为共晶剂,让它和目标化合物通过分子间相互作用结合。原本无序、无法结晶的油状分子,会跟着共晶剂一起有序排列,形成稳定的共晶,长出符合检测要求的高质量单晶。[3]
共晶剂添加法是引入一种结构已知、易于结晶的“伴侣分子”作为共晶剂,让它和目标化合物通过分子间相互作用结合。原本无序、无法结晶的油状分子,会跟着共晶剂一起有序排列,形成稳定的共晶,长出符合检测要求的高质量单晶。[3]
在后续结构解析中,因为共晶剂的结构完全已知,我们可以直接从衍射数据中将其精准区分、扣除,从而还原出目标分子的准确三维结构。
目前有哪些共晶剂已成熟应用?
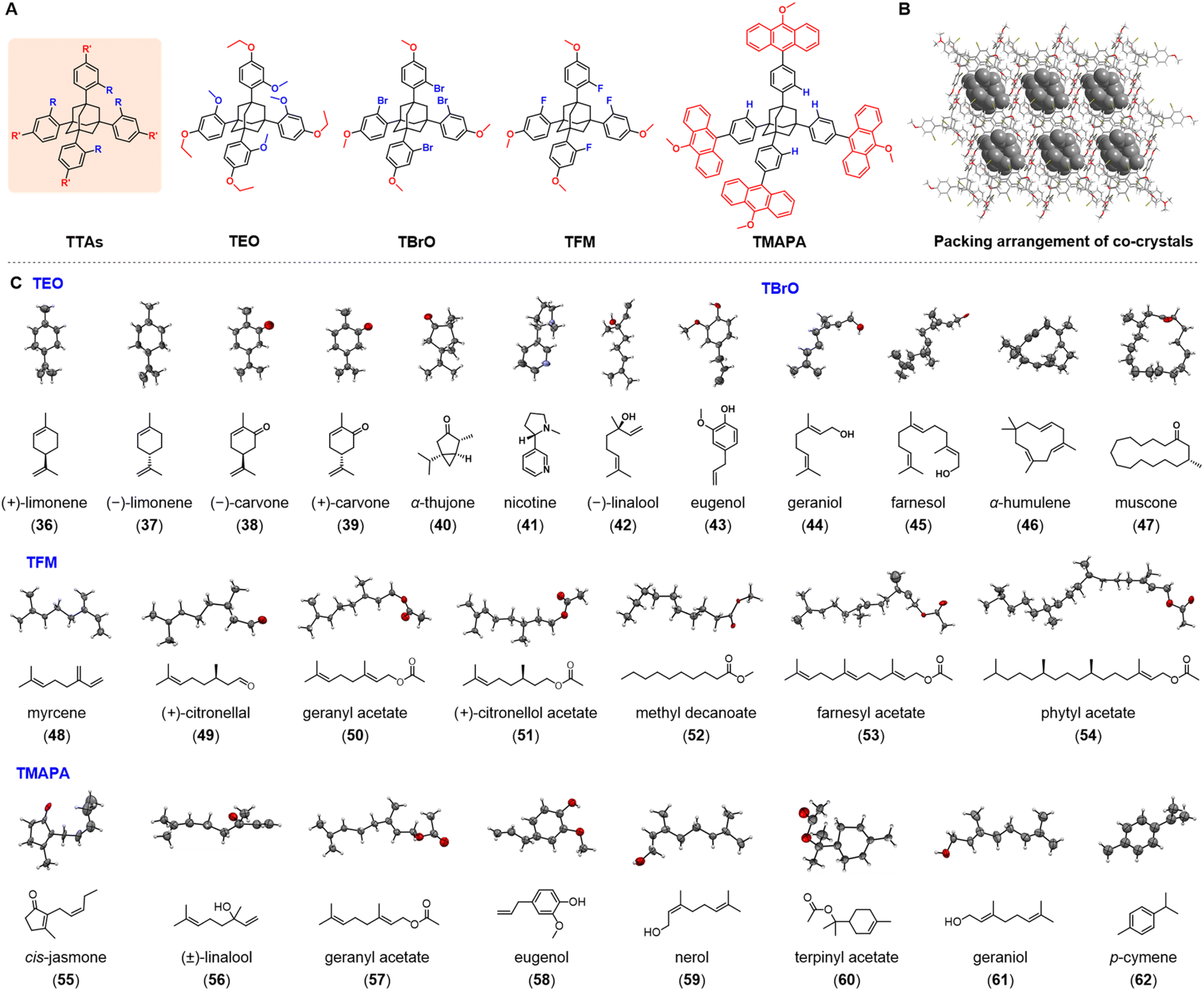
共晶的堆积排列 [5]
共晶剂是一类结构已知、易于结晶且能与目标分子形成分子间相互作用的辅助分子,本质属于功能性小分子或类小分子材料。这类材料由有机基团或离子通过分子间作用力(氢键、范德华力等)与目标分子结合,具备结晶性能优异、结构可精准区分、适配性广的特点。常见的如TDA、苯甲酸、烟酰胺等,因适配性广、结晶效率高,已在多个药物研发项目中成功应用。[4]
共晶剂添加法技术优势:
l 无需筛选合适的溶剂或结晶条件
l 实验周期较短,可快速获得结果
l 适用于油状分子、柔性分子
青云瑞晶案例分享:
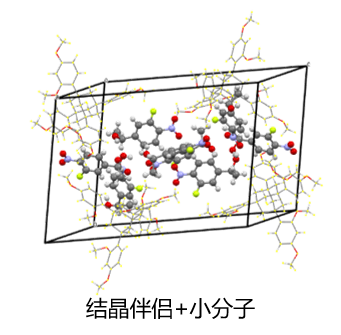
针对某高柔性油状药物分子,我们评估项目情况之后,选择使用TDA作为共晶剂,通过共结晶作用将目标分子稳定嵌入晶格,成功制备出高质量的共晶单晶。在后续结构解析中,我们直接从衍射数据中将其有效区分,通过扣除已知结构的TDA共晶剂,准确确证了该药物分子结构。

#3全场景技术覆盖,助力药物研发突破结构瓶颈
青云瑞晶拥有丰富的单晶培养经验,不仅掌握常规单晶培养手段,更具备晶体海绵法、共晶剂添加法、微量单晶培养等非常规核心技术。凭借多年在疑难样品结构确证领域的项目经验,我们针对油状分子、高柔性分子、微量样品、难结晶粉末等各类棘手样品,都可以提供定制化结构解析方案。全面的单晶培养技术手段,能够全方位覆盖药物研发中的结构确证需求,提供专业的X射线衍射和MicroED结构解析服务,助力客户快速突破结构确证瓶颈。
联系我们,获取更多技术案例与服务详情,让每一个“油状物”挑战,都转化为清晰、合规、可用于申报的确证数据,助力药物研发项目高效推进。
★ 参考文献
[1]ZIGON N, DUPLAN V, WADA N, et al. Crystalline Sponge Method: X-ray Structure Analysis of Small Molecules by Post-Orientation within Porous Crystals—Principle and Proof-of-Concept Studies[J]. Angewandte Chemie International Edition, 2021, 60(48):25204-25222. DOI:10.1002/anie.202106184.
[2]WANG X N, ZHAO Y M, KIRCHON A, et al. Regulating the Topologies of Zirconium–Organic Frameworks for a Crystal Sponge Applicable to Inorganic Matter[J]. Inorganic Chemistry, 2020, 59(17):11940-11944. DOI:10.1021/acs.inorgchem.0c02152.
[3]AAKERÖY C B, SCHULTZ A, SPITTLER S. Crystal engineering of pharmaceutical cocrystals: recent advances [J]. Chemical Society Reviews, 2021, 50 (2): 1383–1410. DOI:10.1039/D0CS01204A
[4]HOSONO N, KITAGAWA C, TANAKA D, et al. Absolute configuration of small molecules by cocrystallization with tetraaryladamantanes [J]. Angewandte Chemie International Edition, 2020, 59 (31): 12976–12982. DOI:10.1002/anie.202004992
[5]SONG J G, YE W C, WANG Y, et al. Advanced crystallography for structure determination of natural products[J]. Natural Product Reports, 2025, 42: 429-442. DOI:10.1039/d4np00071d.